 |
 |
- Search
| Neonatal Med > Volume 27(3); 2020 > Article |
|
Abstract
Purpose
Patent ductus arteriosus (PDA) is associated with increased mortality and morbidities such as intraventricular hemorrhage, necrotizing enterocolitis, bronchopulmonary dysplasia, and neurodevelopmental impairment. The objective of this study was to evaluate mortality and morbidities according to the time of PDA closure.
Methods
For this study, 117 preterm infants with gestational age (GA) of <30 weeks who had PDA were enrolled and allocated to two groups according to the time of PDA closure as follows: early closed group (n=40, PDA closure in <14 days after birth) and delayed closed group (n=77, PDA closure in Ōēź14 days after birth).
Results
GA was higher in the early closed group than in the delayed closed group (27.2┬▒1.6 weeks vs. 26.3┬▒1.7 weeks, P=0.005). Other demographic factors, such as birth weight, Apgar score, and maternal status were not significantly different between the two groups. The incidence rates of surfactant redosing, retinopathy of prematurity (stage ŌēźII), necrotizing enterocolitis (stage ŌēźII), moderate to severe bronchopulmonary dysplasia, and mortality were similar between the two groups. The total durations of mechanical ventilation, invasive ventilation, and hospital stay were longer in the delayed closed group than in the early closed group. However, these became similar after adjustment for GA. The incidence rate of intraventricular hemorrhage (grade ŌēźIII) was significantly higher in the early closed group than in the delayed closed group after adjustment for GA (25.0% vs. 13.0%, adjusted P for GA=0.021).
ļÅÖļ¦źĻ┤ĆņØĆ Ēā£ņāØĻĖ░ņŚÉļŖö ņÜ░ņŗ¼ņŗż ļ░ĢņČ£ļ¤ēņØś ļīĆļČĆļČäņØä ļīĆļÅÖļ¦źņ£╝ļĪ£ ļ│┤ļé┤ļŖö ņżæņÜöĒĢ£ ņŚŁĒĢĀņØä ĒĢśņ¦Ćļ¦ī ņČ£ņāØ Ēøä ĒÅÉņł£ĒÖśņØ┤ ņŗ£ņ×æļÉ©ņŚÉ ļö░ļØ╝ ļČłĒĢäņÜöĒĢ┤ņ¦Ćļ®░, ĒÅēĒÖ£ĻĘ╝ņØś ņłśņČĢĻ│╝ ĒÅēĒÖ£ĻĘ╝ņØś ĒŚłĒśłņä▒ ņĀĆņé░ņåīņ”ØņØ┤ ņ¦äĒ¢ēļÉśļ®┤ņä£ ĒÅÉņćäļÉ£ļŗż[1]. ļÅÖļ¦źĻ┤ĆņØĆ ļ¦īņéŁ ņŗĀņāØņĢäņŚÉņä£ļŖö ņāØĒøä 48ņŗ£Ļ░ä ņØ┤ļé┤ņŚÉ 90%ņŚÉņä£ ĻĖ░ļŖźņĀüņ£╝ļĪ£ ĒÅÉņćäļÉśļ®░ ņØ┤ĒøäņŚÉ ĒĢ┤ļČĆĒĢÖņĀüņ£╝ļĪ£ ņÖäņĀäĒ׳ ĒÅÉņćäļÉ£ļŗż[1]. ņØ┤ļ¤¼ĒĢ£ ĒÅÉņćä ĻĖ░ņĀäņØĆ 35ņŻ╝ ņĀĢļÅäņŚÉ ņÖäņĀäĒ׳ ņä▒ņłÖļÉśņ¦Ćļ¦ī, ļ»ĖņłÖņĢäļŖö ĒÅÉņćä Ļ│╝ņĀĢņŚÉ ļīĆĒĢ£ ļ»╝Ļ░ÉļÅäĻ░Ć ļ¢©ņ¢┤ņ¦ĆĻ│Ā, ņé░ņåī ļīĆņé¼Ļ░Ć ņŚŁņäżņĀüņ£╝ļĪ£ ĒöäļĪ£ņŖżĒāĆĻĖĆļ×Ćļöś E2 (prostaglandin E2) ņāØņä▒ņØä ņ×ÉĻĘ╣ĒĢśĻ│Ā, ļÅÖļ¦źĻ┤ĆņØś ĒÖĢņןņØä ņĢ╝ĻĖ░ĒĢ┤ņä£ ĒÅÉņćä Ļ│╝ņĀĢņØ┤ ņ¦ĆņŚ░ļÉśĻ▒░ļéś ĒÅÉņćä Ēøä ņ×¼Ļ░£ļ░®ļÉśļŖö Ļ▓ĮņÜ░Ļ░Ć ļ¦Äļŗż[2]. ļö░ļØ╝ņä£ ļÅÖļ¦źĻ┤ĆĻ░£ņĪ┤ņ”ØņØĆ ņ┤łļ»ĖņłÖņĢäņŚÉņä£ Ļ░Ćņן ĒØöĒĢ£ ņŗ¼ņןņāüĒā£ļĪ£, ņ×¼Ēā£ņŚ░ļĀ╣(gestational age, GA) 29ņŻ╝ ļ»Ėļ¦ī ļ»ĖņłÖņĢäņØś 40%-60%ņŚÉņä£ ļ░£ņāØĒĢśļ®░[3] GA 28ņŻ╝ ļ»Ėļ¦ī ļ»ĖņłÖņĢäņØś 70%ņŚÉņä£ ļ░£ņāØĒĢ£ļŗż[4].
ļ»ĖņłÖņĢäņŚÉņä£ ļÅÖļ¦źĻ┤ĆĻ░£ņĪ┤ņ”ØņØĆ ņ▓┤ņł£ĒÖśņŚÉņä£ ĒÅÉņł£ĒÖśņ£╝ļĪ£ņØś ļŗ©ļØĮņØä ņ£Āļ░£ĒĢśĻ│Ā, ĻĘĖ Ļ▓░Ļ│╝ ņ▓┤ņł£ĒÖśņØś Ēśłļźśļ¤ē Ļ░ÉņåīņÖĆ ĒÅÉņł£ĒÖśņØś Ēśłļźśļ×æ ņ”ØĻ░ĆļĪ£ ņØĖĒĢ┤ ĒÅÉņåÉņāüņØä ņĢ╝ĻĖ░ĒĢśļ®░, ĒÅÉņČ£Ēśł, ĻĖ░Ļ┤Ćņ¦ĆĒÅÉņØ┤ĒśĢņä▒ņ”ØņØś ņ£äĒŚśņä▒ņØä ņ”ØĻ░Ćņŗ£Ēé©ļŗż[5]. ļśÉĒĢ£ ņ▓┤ņł£ĒÖś ĒśłļźśņØś Ļ░ÉņåīļŖö ņŻ╝ņÜö ņןĻĖ░ ļČĆņĀäņØä ņØ╝ņ£╝Ēéżļ®░ Ļ┤┤ņé¼ņä▒ ņןņŚ╝[6], ļćīņŗżļé┤ņČ£Ēśł[7]ņØś ņ£äĒŚśņØä ņ”ØĻ░Ćņŗ£Ēé©ļŗż. ļö░ļØ╝ņä£ ņØ┤ņĀäņŚÉļŖö ļ»ĖņłÖņĢäņØś ņśłĒøä Ē¢źņāüņØä ņ£äĒĢ┤ ļÅÖļ¦źĻ┤ĆĻ░£ņĪ┤ņ”ØņØä ņāØĒøä ņ┤łĻĖ░ņŚÉ ņĢĮļ¼╝ ļśÉļŖö ņłśņłĀņĀü ļ░®ļ▓Ģņ£╝ļĪ£ ĒÅÉņćäĒĢśļŖö Ļ▓āņØä ļ¬®Ēæ£ļĪ£ ĒĢśņśĆļŗż[8].
ĻĘĖļ¤¼ļéś ņØĖļÅäļ®öĒāĆņŗĀ, ņØ┤ļČĆĒöäļĪ£ĒÄ£Ļ│╝ Ļ░ÖņØĆ ļÅÖļ¦źĻ┤Ć ĒÅÉņćäņŚÉ ņé¼ņÜ®ļÉśļŖö ņĢĮļ¼╝ņØĆ ļ»ĖņłÖņĢäņŚÉņä£ ļćī, ņן, ņŗĀņןņ£╝ļĪ£ņØś Ēśłļźśļź╝ Ļ░Éņåīņŗ£Ēéżļ®░[9], ļ»ĖņłÖņĢäņŚÉņä£ ņāØĒøä ņ┤łĻĖ░ņØś ņłśņłĀņØĆ ņłśņłĀ ĒĢ®ļ│æņ”ØĻ│╝ ļ¦łņĘ© Ļ┤ĆļĀ© ĒśłņŚŁĒĢÖņĀü ļ░Å ĒśĖĒØĪĻĖ░ ĒĢ®ļ│æņ”ØņØä ņ£Āļ░£ĒĢśļ®░ ļ░£ļŗ¼ ņ¦ĆņŚ░ņØś ņ£äĒŚś ļśÉĒĢ£ ņ”ØĻ░Ćņŗ£Ēé©ļŗżĻ│Ā ļ│┤Ļ│ĀļÉśĻ│Ā ņ׳ļŗż[10].
ņĄ£ĻĘ╝ņŚÉļŖö ņ¦ĆņåŹļÉśļŖö ļÅÖļ¦źĻ┤ĆĻ░£ņĪ┤ņ”ØĻ│╝ ļ»ĖņłÖņĢäņØś ņśłĒøä ņé¼ņØ┤ņŚÉ ņāüĻ┤ĆĻ┤ĆĻ│äĻ░Ć ņŚåļŗżļŖö ņŚ░ĻĄ¼ Ļ▓░Ļ│╝Ļ░Ć ļ░£Ēæ£ļÉśĻ│Ā ņ׳ņ£╝ļ®░[11], ļśÉĒĢ£ ņĄ£ĻĘ╝ ļÅÖļ¦źĻ┤ĆņØä ņĢĮļ¼╝ņØ┤ļéś ņłśņłĀņĀü ņ╣śļŻīļ▓Ģņ£╝ļĪ£ ĒÅÉņćäĒĢśņ¦Ć ņĢŖĻ│Ā ņłśņĢĪ ņĀ£ĒĢ£ņØä ĒåĄĒĢ£ ļ│┤ņĪ┤ņĀü ņĀæĻĘ╝ļ▓Ģņ£╝ļĪ£ ņśłĒøäļź╝ Ē¢źņāüņŗ£Ēé© Ļ▓░Ļ│╝ļōżņØ┤ ļ░£Ēæ£ļÉśļ®┤ņä£[12] ļÅÖļ¦źĻ┤ĆĻ░£ņĪ┤ņ”ØņØä ņ¢ĖņĀ£ ņ╣śļŻīĒĢĀņ¦Ć, ņĢĮļ¼╝ņØ┤ļéś ņłśņłĀņĀü Ļ▓░ņ░░ņłĀ ļō▒ ņ¢┤ļ¢ż ļ░®ļ▓Ģņ£╝ļĪ£ ņ╣śļŻīĒĢĀņ¦Ć ņĀĢĒĢśļŖö Ļ▓āņØĆ ņŚ¼ņĀäĒ׳ ļģ╝ļ×ĆņØś ņŚ¼ņ¦ĆĻ░Ć ņ׳ļŗż.
ņØ┤ ņŚ░ĻĄ¼ņŚÉņä£ļŖö ļÅÖļ¦źĻ┤ĆĻ░£ņĪ┤ņ”ØņØ┤ ņ׳ļŖö ļ»ĖņłÖņĢäņŚÉņä£ ļÅÖļ¦źĻ┤Ć ĒÅÉņćä ņŗ£ĻĖ░ņŚÉ ļö░ļźĖ ļćīņŗżļé┤ņČ£Ēśł, ĻĖ░Ļ┤Ćņ¦ĆĒÅÉņØ┤ĒśĢņä▒ņ”Ø, Ļ┤┤ņé¼ņä▒ ņןņŚ╝, ļ»ĖņłÖņĢä ļ¦Øļ¦ēņ”Ø ļō▒ņØś ņśłĒøäņÖĆ ņé¼ļ¦ØļźĀņŚÉ ņ░©ņØ┤Ļ░Ć ņ׳ļŖöņ¦Ć ņĢīņĢäļ│┤Ļ│Āņ×É ĒĢ£ļŗż.
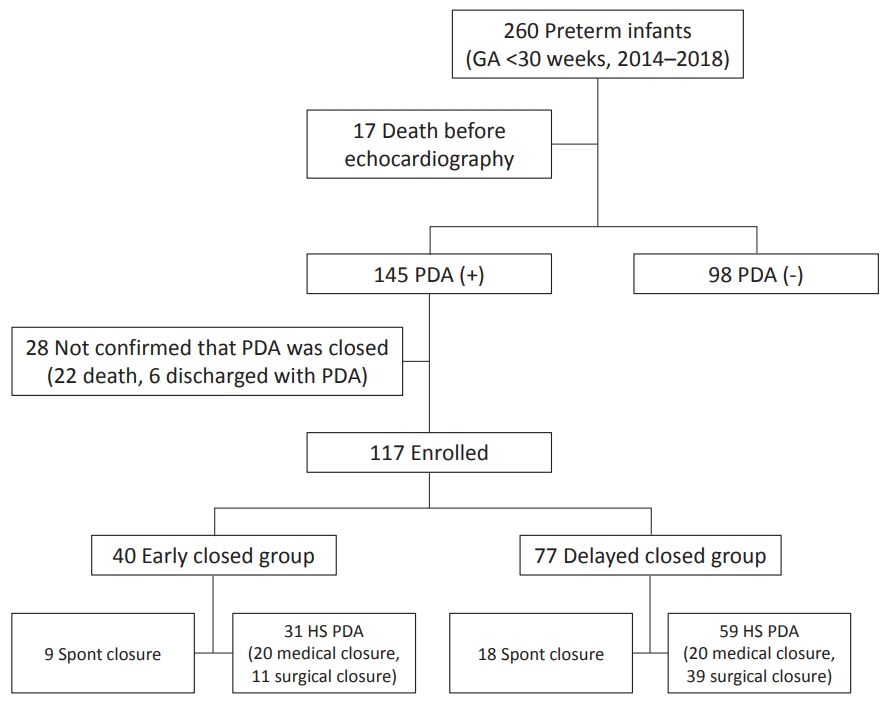
2014ļģä 1ņøöļČĆĒä░ 2018ļģä 12ņøöĻ╣īņ¦Ć ņØĖņĀ£ļīĆĒĢÖĻĄÉ ņØśĻ│╝ļīĆĒĢÖ ļČĆņé░ļ░▒ļ│æņøÉ ņŗĀņāØņĢä ņ¦æņżæņ╣śļŻīņŗżņŚÉ ņ×ģņøÉĒĢ£ GA 30ņŻ╝ ļ»Ėļ¦īņØś ļ»ĖņłÖņĢä ņżæ ļÅÖļ¦źĻ┤ĆĻ░£ņĪ┤ņ”ØņØ┤ ņ¦äļŗ©ļÉ£ ĒÖśņ×É 145ļ¬ģ ņżæ, ļÅÖļ¦źĻ┤ĆņØ┤ ņŚ┤ļ”░ ņ▒ä Ēć┤ņøÉ Ēøä ņÖĖļלņŚÉņä£ ĒÅÉņćä ņŚ¼ļČĆĻ░Ć ĒÖĢņØĖļÉśņ¦Ć ņĢŖņØĆ ĒÖśņ×É 6ļ¬ģĻ│╝ ĒÅÉņćä ņŚ¼ļČĆļź╝ ĒÖĢņØĖĒĢśņ¦Ć ļ¬╗ĒĢśĻ│Ā ņé¼ļ¦ØĒĢ£ ĒÖśņ×É 22ļ¬ģņØä ņĀ£ņÖĖĒĢ£ 117ļ¬ģņØä ļīĆņāüņ£╝ļĪ£ ĒĢśņśĆļŗż(Figure 1).
117ļ¬ģņØś ĒÖśņ×ÉņØś ņØśļ¼┤ĻĖ░ļĪØņØä ĒøäĒ¢źņĀüņ£╝ļĪ£ ļČäņäØĒĢśņŚ¼ ņāØĒøä 14ņØ╝ ņØ┤ņĀäņŚÉ ļÅÖļ¦źĻ┤ĆņØ┤ ĒÅÉņćäļÉ£ ĻĄ░ņØä ņĪ░ĻĖ░ĒÅÉņćäĻĄ░(40ļĪĆ)ņ£╝ļĪ£, ņāØĒøä 14ņØ╝ļČĆĒä░ ĻĘĖ ņØ┤ĒøäņŚÉ ĒÅÉņćäļÉ£ ĻĄ░ņØä ņ¦ĆņŚ░ĒÅÉņćäĻĄ░(77ļĪĆ)ņ£╝ļĪ£ ņĀĢņØś[13]ĒĢśņśĆņ£╝ļ®░ ĒÅÉņćä ņŗ£ĻĖ░ņŚÉ ļö░ļźĖ ļæÉ ĻĄ░ Ļ░äņØś ĒŖ╣ņ¦Ģ ļ░Å ņśłĒøäļź╝ ņĢīņĢäļ│┤ņĢśļŗż.
ņØĖĻĄ¼ ĒåĄĻ│äĒĢÖņĀü ņÜöņØĖņ£╝ļĪ£ GA, ņČ£ņāØņ▓┤ņżæ, ņä▒ļ│ä, 1ļČä ļ░Å 5ļČä ņĢäĒöäĻ░Ć ņĀÉņłś ļō▒ņØś ņČ£ņāØļĀźĻ│╝ ņé░ļ¬©ņØś ņ×äņŗĀņä▒ Ļ│ĀĒśłņĢĢ, ņ×äņŗĀņä▒ ļŗ╣ļć©, ņé░ņĀä ņŖżĒģīļĪ£ņØ┤ļō£ ņé¼ņÜ® ņŚ¼ļČĆ, ņĪ░ņ¦üĒĢÖņĀüņ£╝ļĪ£ ĒÖĢņ¦äļÉ£ ņ£Ąļ¬©ņ¢æļ¦ēņŚ╝ ņ£Āļ¼┤ ļō▒ņØä ņĪ░ņé¼ĒĢśņśĆļŗż. ņśłĒøäņØĖņ×ÉļŖö ņŗĀņāØņĢä ĒśĖĒØĪĻ│żļ×Ćņ”ØĒøäĻĄ░, ĒÅÉĻ│äļ®┤ĒÖ£ņä▒ņĀ£ņØś 2ņ░© Ēł¼ņŚ¼ ņŚ¼ļČĆ, ļćīņŗżļé┤ņČ£Ēśł, ļ»ĖņłÖņĢä ļ¦Øļ¦ēņ”Ø, Ļ┤┤ņé¼ņä▒ ņןņŚ╝, ĻĖ░Ļ┤Ćņ¦ĆĒÅÉņØ┤ĒśĢņä▒ņ”Ø, ņØĖĻ│ĄĒÖśĻĖ░ ņ╣śļŻīĻĖ░Ļ░ä, ņ╣©ņŖĄņĀü ņØĖĻ│ĄĒÖśĻĖ░ ņ╣śļŻīĻĖ░Ļ░ä, ņ×ģņøÉĻĖ░Ļ░ä, ņ×ģņøÉ ņżæ ņé¼ļ¦ØļźĀņØä ņĪ░ņé¼ĒĢśņśĆļŗż.
ņŚ░ĻĄ¼ ļīĆņāü ĒÖśņ×ÉļōżņØĆ ņČ£ņāØ Ēøä ņ▓½ 1ņŻ╝ņØ╝ ņØ┤ļé┤ņŚÉ ņŗ¼ņןņ┤łņØīĒīī(Vivid S5, GE Healthcare, Chicago, IL, USA)ļź╝ ņŗ£Ē¢ēĒĢśņśĆņ£╝ļ®░, ĒśłņŚŁĒĢÖņĀüņ£╝ļĪ£ ņØśļ»Ė ņ׳ļŖö ļÅÖļ¦źĻ┤ĆĻ░£ņĪ┤ņ”Ø(hemodynamically significant patent ductus arteriosus, HS PDA)ņØĆ 2 mm ņØ┤ņāüņØś ņ¦üĻ▓ĮņØä Ļ░Ćņ¦Ćļ®░, ņ┤łņØīĒīīņŚÉņä£ ņĀĆļ¬ģĒĢ£ ņóīņÜ░ ļŗ©ļØĮņØä Ļ░Ćņ¦ĆĻ│Ā ņ׳ļŖö ļÅÖļ¦źĻ┤ĆņØ┤ ņĪ┤ņ×¼ĒĢśļ®░, ņØĖĻ│ĄĒÖśĻĖ░ņØś ļÅäņøĆņØ┤ ĒĢäņÜöĒĢśĻ│Ā ņŗ¼ņ×ĪņØī, ņĀĆĒśłņĢĢ, ļ¦źņĢĢ(ņłśņČĢĻĖ░ ĒśłņĢĢĻ│╝ ņØ┤ņÖäĻĖ░ ĒśłņĢĢņØś ņ░©ņØ┤) ņ”ØĻ░Ć, ĒśĖĒØĪ ņĢģĒÖö ļō▒ ļÅÖļ¦źĻ┤ĆĻ░£ņĪ┤ņ”ØņØä ņŗ£ņé¼ĒĢśļŖö ņ”ØņāüņØ┤ ļÅÖļ░śļÉśļŖö Ļ▓ĮņÜ░ļĪ£ ņĀĢņØśĒĢśņśĆļŗż[12]. ļÅÖļ¦źĻ┤ĆĻ░£ņĪ┤ņ”ØņØ┤ ņ¦äļŗ©ļÉ£ ĒÖśņ×ÉļŖö ņłśņĢĪņĀ£ĒĢ£Ļ│╝ Ļ░ÖņØĆ ļ│┤ņĪ┤ņĀü ņ╣śļŻīļź╝ ņŗ£Ē¢ēĒĢśņśĆņ£╝ļ®░ HS PDAĻ░Ć ņ¦äļŗ©ļÉ£ ĒÖśņ×ÉļŖö ņĢĮļ¼╝ ņ╣śļŻīļź╝ ņŗ£Ē¢ēĒĢśņśĆļŗż. ņĢĮļ¼╝ ņ╣śļŻīņØś ĻĖłĻĖ░ņŚÉ ĒĢ┤ļŗ╣ĒĢśĻ▒░ļéś ņĢĮļ¼╝ ņ╣śļŻī ĒøäņŚÉļÅä HS PDAĻ░Ć ņ¦ĆņåŹļÉśļŖö Ļ▓ĮņÜ░ ņłśņłĀņĀü ņ╣śļŻīļź╝ ņŗ£Ē¢ēĒĢśņśĆļŗż. ņŗ¼ņןņ┤łņØīĒīīņŚÉņä£ HS PDAĻ░Ć ņ¦ĆņåŹļÉśļ®░ ņ×äņāüņĀüņ£╝ļĪ£ HS PDAļĪ£ ņØĖĒĢ£ ņŗ¼ĒÅÉĻĖ░ļŖźņØ┤ ņĢģĒÖöļÉśļŖö Ļ▓ĮņÜ░ņŚÉ HS PDAņØś ņ”ØņāüņØś ņŗ¼ĒĢ£ ņĀĢļÅäņŚÉ ļö░ļØ╝ ņŗĀņāØņĢä ņØśņé¼ņÖĆ ņåīņĢäņŗ¼ņן ņØśņé¼Ļ░Ć ņłśņłĀ ņŚ¼ļČĆļź╝ Ļ▓░ņĀĢĒĢśņśĆļŗż. ļÅÖļ¦źĻ┤ĆĻ░£ņĪ┤ņ”ØņØ┤ ņ¦äļŗ©ļÉśņŚłņ£╝ļéś HS PDAĻ░Ć ņĢäļŗī Ļ▓ĮņÜ░ļŖö 1ņŻ╝ņØ╝ Ēøä ņŗ¼ņןņ┤łņØīĒīī ņČöņĀü Ļ▓Ćņé¼ļź╝ ĒĢśņśĆĻ│Ā, HS PDAļĪ£ ņĢĮļ¼╝ ņ╣śļŻīļź╝ ĒĢ£ Ļ▓ĮņÜ░ļŖö ņĢĮļ¼╝ Ēł¼ņŚ¼ 1ņŻ╝ņØ╝ ņØ┤ļé┤ņŚÉ ņŗ¼ņןņ┤łņØīĒīīļź╝ ņŗ£Ē¢ēĒĢśņśĆņ£╝ļ®░, ņłśņłĀņĀü ņ╣śļŻīļź╝ ĒĢ£ Ļ▓ĮņÜ░ļŖö ĒÖśņ×É ņāüĒā£ņŚÉ ļö░ļØ╝ņä£ 1Ļ░£ņøö Ēøäļéś Ēć┤ņøÉ ņĀäņŚÉ ņŗ¼ņןņ┤łņØīĒīīļź╝ ņŗ£Ē¢ēĒĢśņśĆļŗż.
ņŗĀņāØņĢä ĒśĖĒØĪĻ│żļ×Ćņ”ØĒøäĻĄ░ņØĆ ņŗĀņāØņĢäņØś ĒśĖĒØĪ ņ”Øņāü ļ░Å ĒØēļČĆļ░®ņé¼ņäĀ, ĒśłņĢĪ Ļ░ĆņŖżļČäņäØ Ļ▓░Ļ│╝ņŚÉ ļö░ļØ╝ ņĀĢņØśĒĢśņśĆļŗż[14]. ĻĖ░Ļ┤Ćņ¦ĆĒÅÉņØ┤ĒśĢņä▒ņ”ØņØĆ ņāØĒøä 28ņØ╝ ņØ┤ĒøäņŚÉļÅä ņé░ņåīļéś ņØĖĻ│ĄĒÖśĻĖ░Ļ░Ć ĒĢäņÜöĒĢśĻ│Ā[15], National Institutes of Child Health and Human Development (NICHD) ClassificationņŚÉ ļö░ļØ╝ ņżæņ”ØļÅäļ│äļĪ£ Ļ▓Įņ”Ø, ņżæļō▒ļÅä, ņżæņ”Øņ£╝ļĪ£ ĻĄ¼ļČäĒĢśņśĆņ£╝ļ®░ ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö ņżæļō▒ļÅä ņØ┤ņāüņØś ĻĖ░Ļ┤Ćņ¦ĆĒÅÉņØ┤ĒśĢņä▒ņ”ØņØä ĒżĒĢ©ĒĢśņśĆļŗż. ļćīņŗżļé┤ņČ£ĒśłņØĆ ļćīņ┤łņØīĒīīļź╝ ņØ┤ņÜ®ĒĢ┤ Papile ļō▒[16]ņØś ļČäļźśņŚÉ ļö░ļØ╝ 3ļŗ©Ļ│ä ņØ┤ņāüņØĖ Ļ▓ĮņÜ░ļĪ£ ņĀĢņØśĒĢśņśĆĻ│Ā, Ļ┤┤ņé¼ņä▒ ņןņŚ╝ņØĆ modified Bells staging criteria[17]ņŚÉ ļö░ļØ╝ 2ļŗ©Ļ│ä ņØ┤ņāüņØĖ Ļ▓ĮņÜ░, ļ»ĖņłÖņĢä ļ¦Øļ¦ēņ”ØņØĆ international classification of retinopathy of prematurity ĻĄŁņĀ£ļČäļźśļ▓Ģ[18]ņŚÉ ļö░ļØ╝ 2ļŗ©Ļ│ä ņØ┤ņāüņ£╝ļĪ£ ņĀĢņØśĒĢśņśĆļŗż.
ĒåĄĻ│äļČäņäØņØĆ IBM SPSS Statistics for Windows version 25.0 (IBM Corp., Armonk, NY, USA)ļź╝ ņØ┤ņÜ®ĒĢśņśĆļŗż. ļæÉ ĻĄ░ Ļ░äņØś ņ░©ņØ┤ļŖö ņĀĢĻĘ£ļČäĒżļź╝ ļö░ļź┤ļŖö ņŚ░ņåŹļ│ĆņłśļŖö Student t-test, ņĀĢĻĘ£ļČäĒżļź╝ ļö░ļź┤ņ¦Ć ņĢŖļŖö ņŚ░ņåŹļ│Ćņłśļéś ņØ┤ņé░ļ│ĆņłśļŖö Mann-Whitney U-testļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ļČäņäØĒĢśņśĆĻ│Ā, ļ¬ģļ¬®ļ│ĆņłśļŖö chi-square testļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ļČäņäØĒĢśņśĆļŗż. Ļ┤Ćņ░░Ļ░ÆņØĆ ĒÅēĻĘĀĻ░Æ┬▒Ēæ£ņżĆĒÄĖņ░©ļĪ£ Ēæ£ņŗ£ĒĢśņśĆļŗż. GAņØś ņśüĒ¢źņØä ļ│┤ņĀĢĒĢśĻĖ░ ņ£äĒĢ┤ ņŚ░ņåŹļ│ĆņłśļŖö Ļ│Ąļ│Ćļ¤ēļČäņäØ(analysis of covariance, ANCOVA), ņØ┤ņé░ļ│ĆņłśļŖö ļŗżļ│Ćļ¤ē ļĪ£ņ¦ĆņŖżĒŗ▒ ĒÜīĻĘĆļČäņäØ(multivariate logistic regression)ņØä ņØ┤ņÜ®ĒĢśņśĆļŗż. P Ļ░ÆņØ┤ 0.05 ļ»Ėļ¦īņØĖ Ļ▓ĮņÜ░ļź╝ ĒåĄĻ│äņāü ņ£ĀņØśĒĢ£ Ļ▓āņ£╝ļĪ£ ņĀĢņØśĒĢśņśĆļŗż.
ņ┤Ø 117ļ¬ģņØś ņŚ░ĻĄ¼ļīĆņāü ņżæ ņāØĒøä 14ņØ╝ ņØ┤ņĀäņŚÉ ļÅÖļ¦źĻ┤ĆņØ┤ ĒÅÉņćäļÉ£ ņĪ░ĻĖ░ĒÅÉņćäĻĄ░ņØĆ 34% (40/117), ņāØĒøä 14ņØ╝ļČĆĒä░ ĻĘĖ ņØ┤ĒøäņŚÉ ĒÅÉņćäļÉ£ ņ¦ĆņŚ░ĒÅÉņćäĻĄ░ņØĆ 66% (77/117)ņśĆļŗż. ņĪ░ĻĖ░ĒÅÉņćäĻĄ░ņØś GAĻ░Ć ņ¦ĆņŚ░ĒÅÉņćäĻĄ░ņŚÉ ļ╣äĒĢ┤ ļåÆņĢśņ£╝ļ®░(27.2┬▒1.6ņŻ╝ vs. 26.3┬▒1.7ņŻ╝, P=0.005), ņČ£ņāØņ▓┤ņżæņØĆ ļæÉ ĻĄ░ Ļ░äņØś ņ░©ņØ┤Ļ░Ć ņŚåņŚłļŗż(972.4┬▒264.1 g vs. 945.2┬▒294.5 g, P=0.613). ņä▒ļ│ä, 1ļČä ļ░Å 5ļČä ņĢäĒöäĻ░Ć ņĀÉņłś, ņé░ļ¬©ņØś ņ×äņŗĀņä▒ Ļ│ĀĒśłņĢĢ, ņ×äņŗĀņä▒ ļŗ╣ļć©, ņé░ņĀä ņŖżĒģīļĪ£ņØ┤ļō£ Ēł¼ņŚ¼, ņ£Ąļ¬©ņ¢æļ¦ēņŚ╝ņŚÉņä£ļÅä ļæÉ ĻĄ░ Ļ░äņØś ņ£ĀņØśĒĢ£ ņ░©ņØ┤ļŖö ņŚåņŚłļŗż.
ļÅÖļ¦źĻ┤ĆņØ┤ ĒÅÉņćäļÉśĻĖ░ ņĀäņŚÉ ļ░£ņāØĒĢ£ ĒÅÉņČ£ĒśłĻ│╝ ņĀĆĒśłņĢĢņØĆ ļæÉ ĻĄ░ Ļ░äņØś ņ£ĀņØśĒĢ£ ņ░©ņØ┤ļŖö ņŚåņŚłņ£╝ļ®░(11 [27.5%] vs. 22 [28.6%], P=0.903; 15 [37.5%] vs. 29 [37.7%], P=0.986, respectively) ļÅÖļ¦źĻ┤ĆņØ┤ ĒÅÉņćäļÉśĻĖ░ ņĀäņŚÉ ņ¦äļŗ©ļÉ£ ļćīņŗżļé┤ņČ£ĒśłĻ│╝ Ļ┤┤ņé¼ņä▒ ņןņŚ╝ļÅä ļæÉ ĻĄ░ Ļ░äņØś ņ£ĀņØśĒĢ£ ņ░©ņØ┤ļŖö ņŚåņŚłļŗż(3 [7.5%] vs. 7 [9.1%], P=0.770; 1 [2.5%] vs. 3 [3.9%], P=0.693, respectively).
Ļ░ü ĻĄ░ņØś ņ×ÉņŚ░ ĒÅÉņćä ļ╣äņ£©ņØĆ ņ£ĀņØśĒĢ£ ņ░©ņØ┤Ļ░Ć ņŚåņŚłņ£╝ļéś(9 [22.5%] vs. 18 [23.4%], P=0.915) ņĢĮļ¼╝ ņ╣śļŻī Ēøä ĒÅÉņćäļÉ£ ĒÖśņ×ÉļŖö ņĪ░ĻĖ░ĒÅÉņćäĻĄ░ņŚÉņä£ ļ¦ÄņĢśņ£╝ļ®░(20 [50.0%] vs. 20 [26.0%], P=0.009), ņłśņłĀņĀü ņ╣śļŻīĻ░Ć ĒĢäņÜöĒĢ£ ĒÖśņ×ÉļŖö ņ¦ĆņŚ░ĒÅÉņćäĻĄ░ņŚÉņä£ ļ¦ÄņĢśļŗż(11 [27.5%] vs. 39 [50.6%], P=0.016) (Table 1).
ļ¬©ļōĀ ĒÖśņ×ÉļōżņØ┤ ņŗĀņāØņĢä ĒśĖĒØĪĻ│żļ×Ćņ”ØĒøäĻĄ░ņØä ņ¦äļŗ©ļ░øņĢśņ£╝ļ®░, ĒÅÉĻ│äļ®┤ĒÖ£ņä▒ņĀ£ņØś 2ņ░© Ēł¼ņŚ¼ļŖö Ļ░ü ĻĄ░ Ļ░äņØś ņ░©ņØ┤Ļ░Ć ņŚåņŚłļŗż(4 [10.3%] vs. 10 [13.3%], P=0.635). 3ļŗ©Ļ│ä ņØ┤ņāü ļćīņŗżļé┤ņČ£ĒśłņØĆ ņĪ░ĻĖ░ĒÅÉņćäĻĄ░ņŚÉņä£ 22.6┬▒20.0ņØ╝ņŚÉ ļ░£ņāØĒĢśņśĆĻ│Ā ņ¦ĆņŚ░ĒÅÉņćäĻĄ░ņŚÉņä£ 16.3┬▒12.0ņØ╝ņŚÉ ļ░£ņāØĒĢśņśĆļŗż. ļćīņŗżļé┤ņČ£ĒśłņØĆ GAļź╝ ļ│┤ņĀĢĒ¢łņØä ļĢī ņĪ░ĻĖ░ĒÅÉņćäĻĄ░ņŚÉņä£ ļŹö ļ¦ÄņĢśņ£╝ļ®░ (10 [25.0%] vs. 10 [13.0%], P=0.102, adjusted P for GA=0.021), ļÅÖļ¦źĻ┤Ć ņ╣śļŻīņØś ĒĢ®ļ│æņ”ØņØä ļČäņäØĒĢśĻĖ░ ņ£äĒĢ┤ ļÅÖļ¦źĻ┤Ć ĒÅÉņćä ĒøäņŚÉ ļ░£ņāØĒĢ£ ļćīņŗżļé┤ņČ£Ēśłļ¦ī ļČäņäØĒĢśņśĆņØä ļĢīņŚÉļÅä ņĪ░ĻĖ░ĒÅÉņćäĻĄ░ņŚÉņä£ ļŹö ļ¦ÄņĢśļŗż(7 [17.5%] vs. 3 [3.9%], P=0.013, adjusted P for GA=0.011). ļ»ĖņłÖņĢä ļ¦Øļ¦ēņ”Ø(11 [32.4%] vs. 34 [44.7%], P=0.222, adjusted P for GA=0.453), ĻĖ░Ļ┤Ćņ¦ĆĒÅÉņØ┤ĒśĢņä▒ņ”Ø(5 [15.2%] vs. 19 [26.8%], P=0.191, adjusted P for GA=0.384), ņ×ģņøÉ ņżæ ņé¼ļ¦ØļźĀ(5 [12.5%] vs. 7 [9.1%], P=0.564, adjusted P for GA=0.384)ņØĆ ļæÉ ĻĄ░ Ļ░äņØś ņ£ĀņØśĒĢ£ ņ░©ņØ┤ļŖö ņŚåņŚłļŗż.
Ļ┤┤ņé¼ņä▒ ņןņŚ╝ņØĆ ņĪ░ĻĖ░ĒÅÉņćäĻĄ░ņŚÉņä£ 16.3┬▒12.0ņØ╝ņŚÉ ļ░£ņāØĒĢśņśĆĻ│Ā, ņ¦ĆņŚ░ĒÅÉņćäĻĄ░ņŚÉņä£ 29.0┬▒12.9ņØ╝ņŚÉ ļ░£ņāØĒĢśņśĆļŗż. Ļ┤┤ņé¼ņä▒ ņןņŚ╝ ļśÉĒĢ£ ļæÉ ĻĄ░ Ļ░äņØś ņ░©ņØ┤ļŖö ņŚåņŚłļŗż(4 [10.0%] vs. 7 [9.1%], P=0.873, adjusted P for GA=0.796). ļÅÖļ¦źĻ┤Ć ņ╣śļŻīņØś ĒĢ®ļ│æņ”ØņØä ļČäņäØĒĢśĻĖ░ ņ£äĒĢ┤ņä£ ļÅÖļ¦źĻ┤Ć ĒÅÉņćä ĒøäņŚÉ ļ░£ņāØĒĢ£ Ļ┤┤ņé¼ņä▒ ņןņŚ╝ļ¦ī ļČäņäØĒĢśņśĆņØä ļĢīņŚÉļÅä ļæÉ ĻĄ░ Ļ░äņØś ņ░©ņØ┤Ļ░Ć ņŚåņŚłļŗż(3 [7.5%] vs. 4 [5.2%], P=0.618, adjusted P for GA=0.677). ņØĖĻ│ĄĒÖśĻĖ░ ņ╣śļŻīĻĖ░Ļ░äņØĆ ņĪ░ĻĖ░ĒÅÉņćäĻĄ░ņØ┤ ņ¦ĆņŚ░ĒÅÉņćäĻĄ░ņŚÉ ļ╣äĒĢ┤ ņ¦¦ņĢśņ£╝ļéś GAļź╝ ļ│┤ņĀĢĒĢśņśĆņØä ļĢī ņ£ĀņØśĒĢ£ ņ░©ņØ┤ļŖö ņŚåņŚłļŗż(22.2┬▒19.7 days vs. 37.1┬▒36.1 days, P=0.004, adjusted P for GA=0.247). ņ╣©ņŖĄņĀü ņØĖĻ│ĄĒÖśĻĖ░ ņ╣śļŻīĻĖ░Ļ░ä ļśÉĒĢ£ ņĪ░ĻĖ░ĒÅÉņćäĻĄ░ņŚÉņä£ ņ¦¦ņĢśņ£╝ļéś GAļź╝ ļ│┤ņĀĢĒ¢łņØä ļĢī ņ£ĀņØśĒĢ£ ņ░©ņØ┤ļŖö ņŚåņŚłļŗż(17.3┬▒17.9 days vs. 29.9┬▒29.1 days, P=0.004, adjusted P for GA=0.218). ņ×ģņøÉĻĖ░Ļ░äļÅä ņĪ░ĻĖ░ĒÅÉņćäĻĄ░ņØ┤ ņ¦ĆņŚ░ĒÅÉņćäĻĄ░ņŚÉ ļ╣äĒĢ┤ ņ¦¦ņĢśņ£╝ļéś GAļź╝ ļ│┤ņĀĢĒ¢łņØä ļĢī ņ£ĀņØśĒĢ£ ņ░©ņØ┤ļŖö ņŚåņŚłļŗż(75.7┬▒37.7 days vs. 99.5┬▒39.9 days, P=0.002, adjusted P for GA=0.056) (Table 2).
GAņØś ņśüĒ¢źņØä ļ│┤ņĀĢĒĢśĻĖ░ ņ£äĒĢ┤ Ļ░ü ĻĄ░ņØä GAņŚÉ ļö░ļØ╝ GA 24-26ņŻ╝, GA 27-29ņŻ╝ļĪ£ ņäĖļČäĒĢśņśĆļŗż. ĒÅÉĻ│äļ®┤ĒÖ£ņä▒ņĀ£ņØś 2ņ░© Ēł¼ņŚ¼, ļ»ĖņłÖņĢä ļ¦Øļ¦ēņ”Ø, Ļ┤┤ņé¼ņä▒ ņןņŚ╝, ĻĖ░Ļ┤Ćņ¦ĆĒÅÉņØ┤ĒśĢņä▒ņ”Ø, ņØĖĻ│ĄĒÖśĻĖ░ ņ╣śļŻīĻĖ░Ļ░ä, ņ╣©ņŖĄņĀü ņØĖĻ│ĄĒÖśĻĖ░ ņ╣śļŻīĻĖ░Ļ░äņØĆ ņĪ░ĻĖ░ĒÅÉņćäĻĄ░Ļ│╝ ņ¦ĆņŚ░ĒÅÉņćäĻĄ░ Ļ░ä ņ░©ņØ┤Ļ░Ć ņŚåņŚłļŗż. 3ļŗ©Ļ│ä ņØ┤ņāü ļćīņŗżļé┤ņČ£Ēśł(6 [21.4%] vs. 0 [0.0%], P=0.004)Ļ│╝ ņé¼ļ¦ØļźĀ(4 [14.3%] vs. 0 [0.0%], P=0.021)ņØĆ GA 27-29ņŻ╝ņØś ņĪ░ĻĖ░ĒÅÉņćäĻĄ░ņŚÉņä£ ņ¦ĆņŚ░ĒÅÉņćäĻĄ░ņŚÉ ļ╣äĒĢ┤ņä£ ļåÆņĢśļŗż. ņ×ģņøÉĻĖ░Ļ░äņØĆ GA 27-29ņŻ╝ņØś ņ¦ĆņŚ░ĒÅÉņćäĻĄ░ņŚÉņä£ ļŹö ĻĖĖņŚłļŗż(62.75 ┬▒30.2 vs. 82.54┬▒25.2, P=0.008) (Table 3).
ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö HS PDAņØś ņĪ░ĻĖ░ĒÅÉņćäĻĄ░ņØ┤ ņ¦ĆņŚ░ĒÅÉņćäĻĄ░ņŚÉ ļ╣äĒĢ┤ ļćīņŗżļé┤ņČ£ĒśłņØĆ ļ¦ÄņĢśņ£╝ļéś, ļ»ĖņłÖņĢä ļ¦Øļ¦ēņ”Ø, Ļ┤┤ņé¼ņä▒ ņןņŚ╝, ĻĖ░Ļ┤Ćņ¦ĆĒÅÉņØ┤ĒśĢņä▒ņ”Ø, ņé¼ļ¦ØļźĀņØĆ ņ░©ņØ┤Ļ░Ć ņŚåņŚłļŗż. ņØĖĻ│ĄĒÖśĻĖ░ ņ╣śļŻīĻĖ░Ļ░ä, ņ╣©ņŖĄņĀü ņØĖĻ│ĄĒÖśĻĖ░ ņ╣śļŻīĻĖ░Ļ░äļÅä ņ░©ņØ┤Ļ░Ć ņŚåņŚłļŗż.
ņØ┤ņĀäņŚÉļŖö ļ»ĖņłÖņĢäņØś ņśłĒøä Ē¢źņāüņØä ņ£äĒĢ┤ņä£ ļÅÖļ¦źĻ┤ĆĻ░£ņĪ┤ņ”ØņØä ņāØĒøä ņ┤łĻĖ░ņŚÉ ņ╣śļŻīĒĢśņśĆļŗż. ņóīņÜ░ļŗ©ļØĮņØś ļÅÖļ¦źĻ┤Ćņ£╝ļĪ£ ņØĖĒĢ£ ņóīņŗ¼ņŗż ņĢĢļĀź ņ”ØĻ░ĆļĪ£ ĒÅÉĒśłļźśļ¤ēņØ┤ ņ”ØĻ░ĆĒĢśņŚ¼ ĒÅÉļÅÖļ¦ź ņĢĢļĀźņØ┤ ņ”ØĻ░ĆĒĢśļ®░ ņØ┤ļĪ£ ņØĖĒĢ┤ ĒÅÉ Ļ░äņ¦łļĪ£ņØś ņØ┤Ē¢ēņØ┤ ņ”ØĻ░ĆĒĢśņŚ¼ ĒÅÉļČĆņóģĻ│╝ ĒÅÉņČ£ĒśłņØä ņĢ╝ĻĖ░ĒĢśļ®░ Ēśłņן ļŗ©ļ░▒ņØś ĒÅÉĒżļĪ£ņØś ļłäņČ£ņØĆ ĒÅÉĒæ£ļ®┤ĒÖ£ņä▒ņĀ£ņØś ĻĖ░ļŖźņØä ņ¢ĄņĀ£ĒĢ£ļŗż[4]. ļÅÖļ¦źĻ┤ĆņØś ņĪ░ĻĖ░ĒÅÉņćäĻĄ░ņØ┤ ņ¦ĆņŚ░ĒÅÉņćäĻĄ░ņŚÉ ļ╣äĒĢ┤ ņØĖĻ│ĄĒÖśĻĖ░ ņ╣śļŻīĻĖ░Ļ░äņØ┤ ņ£ĀņØśĒĢśĻ▓ī ņ¦¦ņĢśņ£╝ļ®░[19], ņśłļ░®ņĀüņ£╝ļĪ£ ņāØĒøä ņ┤łĻĖ░ņŚÉ ņØĖļÅäļ®öĒāĆņŗĀņØä Ēł¼ņŚ¼ĒĢ£ ĻĄ░ņØ┤ ņāØĒøä ņØ╝ņŻ╝ņØ╝ ņØ┤ĒøäņŚÉ ĒĢäņÜö ņŗ£ ņ╣śļŻīļź╝ ĒĢ£ ĻĄ░ņŚÉ ļ╣äĒĢ┤ņä£ ņĀĆĒśłņĢĢ ļ░Å ņØĖĻ│ĄĒÖśĻĖ░ ņØśņĪ┤ļÅäĻ░Ć ņĀüņŚłĻ│Ā[20], ĻĖ░Ļ┤Ćņ¦ĆĒÅÉņØ┤ĒśĢņä▒ņ”Ø ļśÉļŖö ņé¼ļ¦ØņØ┤ ņĀüņŚłļŗż[21]. Schena ļō▒[22]ņŚÉ ņØśĒĢśļ®┤ HS PDAņŚÉ ļģĖņČ£ļÉśļŖö ņŗ£Ļ░äņØ┤ 1ņŻ╝ņØ╝ ņ”ØĻ░ĆĒĢĀņłśļĪØ ĻĖ░Ļ┤Ćņ¦ĆĒÅÉņØ┤ĒśĢņä▒ņ”ØņØś ņ£äĒŚśņØ┤ 1.7ļ░░ ņ”ØĻ░ĆĒĢśņśĆņ£╝ļ®░, GA 28ņŻ╝ ļ»Ėļ¦īņŚÉņä£ ņāØĒøä 3ņØ╝ņŚÉ ņĪ┤ņ×¼ĒĢśļŖö Ēü░ ļÅÖļ¦źĻ┤ĆņØĆ ņé¼ļ¦ØļźĀ ļśÉļŖö Ļ│ĀļÅä ļćīņČ£Ēśł, Ļ┤┤ņé¼ņä▒ ņןņŚ╝, ĻĖ░Ļ┤Ćņ¦ĆĒÅÉņØ┤ĒśĢņä▒ņ”ØņØś ņ£äĒŚśņØä ņ”ØĻ░Ćņŗ£ņ╝░ļŗż[23]. ļśÉĒĢ£ ņāØĒøä 3ņŻ╝ ņØ┤ņĀäņŚÉ ļÅÖļ¦źĻ┤ĆĻ░£ņĪ┤ņ”ØņØ┤ ĒÅÉņćäļÉ£ ĻĄ░ņŚÉņä£ ĻĖ░Ļ┤Ćņ¦ĆĒÅÉņØ┤ĒśĢņä▒ņ”Ø, ļćīņŗżļé┤ņČ£Ēśł, ĻĖēņä▒ ņŗĀļČĆņĀäņØś ļ╣łļÅäļź╝ ņżäņśĆĻ│Ā, ņŗĀĻ▓ĮĒĢÖņĀü ņśłĒøäļź╝ Ē¢źņāüņŗ£ņ╝░ļŗż[24].
ĻĘĖļ¤¼ļéś ļÅÖļ¦źĻ┤Ć ĒÅÉņćäņŚÉ ņé¼ņÜ®ĒĢśļŖö ņĢĮļ¼╝ņØĖ ņØĖļÅäļ®öĒāĆņŗĀĻ│╝ ņØ┤ļČĆĒöäļĪ£ĒÄ£ņØĆ ĒöäļĪ£ņŖżĒāĆĻĖĆļ×Ćļöś ĒĢ®ņä▒ņØś ņ¢ĄņĀ£ļź╝ ĒåĄĒĢ┤ ĒśłĻ┤Ć ņłśņČĢņØä ņ┤łļלĒĢśļ®░, ļćī, ņן, ņŗĀņןņ£╝ļĪ£ņØś Ēśłļźśļź╝ Ļ░Éņåī ņŗ£ņ╝£ ļćīņŗżļé┤ņČ£Ēśł, Ļ┤┤ņé¼ņä▒ ņןņŚ╝, ņåīļ│Ćļ¤ē Ļ░Éņåī ļō▒ņØś ļČĆņ×æņÜ®ņØ┤ ņāØĻĖĖ ņłś ņ׳ļŗż[9]. Bourgoin ļō▒[25]ņØś ņŚ░ĻĄ¼ņŚÉņä£ 29ņŻ╝ ļ»Ėļ¦īņØś ļ»ĖņłÖņĢä ņżæ ļÅÖļ¦źĻ┤ĆņØä ņłśņłĀņĀüņ£╝ļĪ£ ĒÅÉņćäĒĢ£ ĒÖśņ×ÉĻĄ░ņŚÉņä£ 2ņäĖņØś ņŗĀĻ▓Įļ░£ļŗ¼ņ¦ĆņŚ░ņØ┤ ļŹö ļ╣łļ▓łĒĢśĻ▓ī ļéśĒāĆļé¼ļŗż. ļśÉĒĢ£ Benitz ļō▒[26]ņØś ņŚ░ĻĄ¼ņŚÉ ļö░ļź┤ļ®┤ ņłśņłĀņĀü ņ╣śļŻīļŖö ņŗĀņåŹĒ׳, ņÖäļ▓ĮĒĢśĻ▓ī ļÅÖļ¦źĻ┤ĆņØä ĒÅÉņćäņŗ£Ēé¼ ņłśļŖö ņ׳ņ¦Ćļ¦ī, ņłśņłĀĻ│╝ ļ¦łņĘ©ņÖĆ Ļ┤ĆļĀ©ļÉ£ ņŗ¼Ļ░üĒĢ£ ĒśłņŚŁĒĢÖņĀü ļśÉļŖö ĒśĖĒØĪĻĖ░ ĒĢ®ļ│æņ”ØņØ┤ ļ░£ņāØĒĢĀ ņłś ņ׳ņ£╝ļ®░ ņØ┤ļĪ£ ņØĖĒĢ┤ ņ¦æņżæ ņ╣śļŻīņŚÉ ļīĆĒĢ£ ĒĢäņÜöĻ░Ć ņ”ØĻ░ĆĒĢśļ®░, ņóīņĖĪņä▒ļīĆ ļśÉļŖö ĒÜĪĻ▓®ļ¦ē ļ¦łļ╣ä, ņ£Āļ»ĖĒØē, ņ▓ÖņČö ņĖĪļ¦īņ”Ø ļō▒Ļ│╝ Ļ░ÖņØĆ ĒĢ®ļ│æņ”ØņØ┤ ņāØĻĖĖ ņłś ņ׳ļŗż. ļö░ļØ╝ņä£ ņĄ£ĻĘ╝ņŚÉļŖö ņłśņĢĪ ņĀ£ĒĢ£, ņŖ╣ņĢĢņĀ£ ņé¼ņÜ®, ņ¢æņĢĢĒÖśĻĖ░ ļō▒ņØś ļ│┤ņĪ┤ņĀüņØĖ ļ░®ļ▓ĢņØä ņØ┤ņÜ®ĒĢ┤ņä£ ļÅÖļ¦źĻ┤ĆņØä ĒåĄĒĢ£ ļŗ©ļØĮņØś ņśüĒ¢źņØä ņĄ£ņåīĒÖöĒĢ©ņ£╝ļĪ£ņŹ© ņĢĮļ¼╝ ņ╣śļŻīļéś ņłśņłĀņĀü ņ╣śļŻīļź╝ ņżäņØ┤ļĀżļŖö ņŚ░ĻĄ¼Ļ░Ć ļ¦ÄņØ┤ ņ¦äĒ¢ēļÉśĻ│Ā ņ׳ļŗż.
ļ»ĖĻĄŁņØś ĒĢ£ ņŚ░ĻĄ¼ņŚÉņä£ļŖö 28ņŻ╝ ļ»Ėļ¦īņØś ļ»ĖņłÖņĢäņŚÉņä£ ļÅÖļ¦źĻ┤ĆĻ░£ņĪ┤ņ”ØņØś ņ╣śļŻīņÖĆ ņé¼ļ¦ØļźĀ Ļ░äņØś ņāüĻ┤ĆĻ┤ĆĻ│äĻ░Ć ņŚåņŚłņ£╝ļ®░[27], ņĢĮļ¼╝ļĪ£ ļÅÖļ¦źĻ┤Ć ĒÅÉņćäņŚÉ ņŗżĒī©ĒĢ£ ĒÖśņ×ÉņŚÉņä£ Ļ▓░ņ░░ņłĀņØä ņŗ£Ē¢ēĒĢ£ ĻĄ░Ļ│╝ Ļ▓░ņ░░ņłĀņØä ņŗ£Ē¢ēĒĢśņ¦Ć ņĢŖņØĆ ĻĄ░ņØä ļ╣äĻĄÉĒĢ£ ņŚ░ĻĄ¼ņŚÉņä£ ņé¼ļ¦Ø ļśÉļŖö ņŗĀĻ▓Įļ░£ļŗ¼ ņåÉņāüņØĆ ņ░©ņØ┤Ļ░Ć ņŚåņŚłļŗż[28]. Sung ļō▒[29]ņØś ņŚ░ĻĄ¼ņŚÉņä£ļŖö ļÅÖļ¦źĻ┤ĆĻ░£ņĪ┤ņ”ØņØä ņĢĮļ¼╝ ļ░Å ņłśņłĀņĀüņ£╝ļĪ£ ņĀüĻĘ╣ņĀüņ£╝ļĪ£ ĒÅÉņćäĒĢ£ ĒÖśņ×ÉĻĄ░ņŚÉ ļ╣äĒĢ┤ ņłśņĢĪ ņĀ£ĒĢ£, ņØ┤ļć©ņĀ£ ņé¼ņÜ® ļō▒ ļ│┤ņĪ┤ņĀü ņ╣śļŻīļź╝ ĒĢ£ ĒÖśņ×ÉĻĄ░ņŚÉņä£ ĻĖ░Ļ┤Ćņ¦ĆĒÅÉņØ┤ĒśĢņä▒ņ”ØņØś ļ╣łļÅäĻ░Ć ļé«ņĢśņ£╝ļ®░, ņ×ģņøÉ ņżæ ņé¼ļ¦ØļźĀ, ļćīņŗżļé┤ņČ£Ēśł, ļéŁĒżņä▒ ļ░▒ņ¦łņŚ░ĒÖöņ”Ø, ļ»ĖņłÖņĢä ļ¦Øļ¦ēņ”ØņØĆ ļÅÖļ¦źĻ┤ĆĻ░£ņĪ┤ņ”ØņØś ņ╣śļŻī ļ░®ļ▓ĢņŚÉ ļö░ļźĖ ņ£ĀņØśĒĢ£ ņ░©ņØ┤Ļ░Ć ņŚåņŚłļŗż. Jhaveri ļō▒[30]ņØś ņŚ░ĻĄ¼ņŚÉņä£ļŖö ļÅÖļ¦źĻ┤ĆĻ░£ņĪ┤ņ”ØņŚÉ ļīĆĒĢ┤ ņāØĒøä ņ┤łĻĖ░ņŚÉ ņĀüĻĘ╣ņĀüņ£╝ļĪ£ ņ╣śļŻīĒĢ£ ĒÖśņ×ÉĻĄ░ņŚÉ ļ╣äĒĢ┤ ļ│┤ņĪ┤ņĀü ņ╣śļŻīļź╝ ĒĢ£ ĒÖśņ×ÉĻĄ░ņŚÉņä£ Ļ┤┤ņé¼ņä▒ ņןņŚ╝ņØś ļ╣łļÅäĻ░Ć ļŹö ļé«ņĢśņ£╝ļ®░, ĻĖ░Ļ┤Ćņ¦ĆĒÅÉņØ┤ĒśĢņä▒ņ”Ø, Ēī©Ēśłņ”Ø, ļ»ĖņłÖņĢä ļ¦Øļ¦ēņ”Ø, ņŗĀĻ▓ĮņåÉņāü, ņé¼ļ¦ØļźĀņØĆ Ļ░ü ĒÖśņ×ÉĻĄ░ņØś ņ£ĀņØśĒĢ£ ņ░©ņØ┤Ļ░Ć ņŚåņŚłļŗż. ļ»ĖņłÖņĢäņØś HS PDAļź╝ ņ¢ĖņĀ£, ņ¢┤ļ¢ż ļ░®ļ▓Ģņ£╝ļĪ£ ņ╣śļŻīĒĢ┤ņĢ╝ ĒĢśļŖöņ¦ĆļŖö ņĢäņ¦ü ļģ╝ļ×ĆņØś ņŚ¼ņ¦ĆĻ░Ć ņ׳ņ¦Ćļ¦ī, ņ”ØņāüņØ┤ ņŚåļŖö ļ»ĖņłÖņĢäņŚÉņä£ ņāØĒøä ņ┤łļ░śņŚÉ ņśłļ░®ņĀüņ£╝ļĪ£ ņØ╝Ļ┤äņĀüņ£╝ļĪ£ ņ╣śļŻīļź╝ ĒĢśļŖö Ļ▓āņØĆ ļ»ĖņłÖņĢäņØś ņןĻĖ░ņĀüņØĖ ņśłĒøä Ē¢źņāüņŚÉ ļÅäņøĆņØ┤ ļÉśņ¦Ć ņĢŖņ£╝ļ®░ ņśżĒ׳ļĀż ņ╣śļŻīņÖĆ Ļ┤ĆļĀ©ļÉ£ ĒĢ®ļ│æņ”ØņØä ņ”ØĻ░Ćņŗ£Ēé¼ ņ£äĒŚśņØ┤ ņ׳ņ¢┤ņä£ ĻČīĒĢśņ¦Ć ņĢŖļŖöļŗż[26].
ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö ņĪ░ĻĖ░ĒÅÉņćäĻĄ░ņŚÉņä£ ļćīņŗżļé┤ņČ£ĒśłņØś ļ╣łļÅäĻ░Ć ļåÆņĢśņ£╝ļ®░, ļÅÖļ¦źĻ┤Ć ĒÅÉņćä ĒøäņŚÉ ļ░£ņāØĒĢ£ ļćīņŗżļé┤ņČ£ĒśłņØś ļ╣łļÅäļÅä ļåÆņĢśĻ│Ā GA 27-29ņŻ╝ņØś ņĪ░ĻĖ░ĒÅÉņćäĻĄ░ņŚÉņä£ ļćīņŗżļé┤ņČ£Ēśł, ņé¼ļ¦ØļźĀņØ┤ ļåÆņĢśļŗż. ņØ┤ļŖö ņāØĒøä ņ┤łĻĖ░ņŚÉ ņĢĮļ¼╝ Ēś╣ņØĆ ņłśņłĀņØä ĒåĄĒĢ┤ ņĀüĻĘ╣ņĀüņ£╝ļĪ£ ņ╣śļŻīĒĢśņśĆņØä ļĢī HS PDAņŚÉ ļģĖņČ£ļÉśļŖö ĻĖ░Ļ░äņØĆ ņżäņ¢┤ļōżņ¦Ćļ¦ī ņ╣śļŻīņØś ļČĆņ×æņÜ®ņØä Ļ░äĻ│╝ĒĢĀ ņłśļŖö ņŚåņØīņØä ņŗ£ņé¼ĒĢśļŖö ņåīĻ▓¼ņØ┤ļ®░, ņØ┤ņŚÉ ļīĆĒĢ┤ņä£ļŖö Ē¢źĒøä ņČöĻ░ĆņĀüņØĖ ņŚ░ĻĄ¼Ļ░Ć ĒĢäņÜöĒĢĀ Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż.
ļ│Ė ņŚ░ĻĄ¼ļŖö ļ¬ć Ļ░Ćņ¦Ć ņĀ£ĒĢ£ņĀÉņØä Ļ░Ćņ¦ĆĻ│Ā ņ׳ļŗż. ļæÉ ĻĄ░ Ļ░äņŚÉ ņ░©ņØ┤Ļ░Ć ņ׳ļŖö GAļŖö ļ│┤ņĀĢĒĢśņśĆņ£╝ļéś, ĒøäĒ¢źņĀü ņŚ░ĻĄ¼ņØ┤ĻĖ░ ļĢīļ¼ĖņŚÉ GA ņÖĖņŚÉļÅä ņśłĒøäņŚÉ ņśüĒ¢źņØä ņżä ņłś ņ׳ļŖö ļŗżļźĖ ņÜöņØĖļōżņØ┤ ņ׳ņØä Ļ░ĆļŖźņä▒ņØ┤ ņ׳ļŗż. ņŗ¼ņןņ┤łņØīĒīī ņŗ£Ē¢ē ņĀä ņé¼ļ¦ØĒĢ£ 17ļ¬ģĻ│╝ ņŗ¼ņןņ┤łņØīĒīīļĪ£ ļÅÖļ¦źĻ┤ĆĻ░£ņĪ┤ņ”ØņØ┤ ņ¦äļŗ©ļÉśņŚłņ£╝ļéś ĒÅÉņćä ņŚ¼ļČĆļź╝ ĒÖĢņØĖĒĢśņ¦Ć ļ¬╗ĒĢśĻ│Ā ņé¼ļ¦ØĒĢ£ 22ļ¬ģņØä ņĀ£ņÖĖĒĢśĻ│Ā ĒÅÉņćä ņŚ¼ļČĆļź╝ ĒÖĢņØĖĒĢĀ ņłś ņ׳ņŚłļŹś ĒÖśņ×ÉņØś ņé¼ļ¦ØļźĀņØä ļ╣äĻĄÉĒĢśņśĆļŖöļŹ░ ņĀ£ņÖĖļÉ£ ĒÖśņ×ÉņØś ņé¼ļ¦ØĻ│╝ HS PDAņØś Ļ┤ĆļĀ©ņä▒ļÅä ņ׳ņØä Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż. ņĢĮļ¼╝ ņ╣śļŻīņØś ĻĖłĻĖ░ņŚÉ ĒĢ┤ļŗ╣ĒĢśĻ▒░ļéś ņĢĮļ¼╝ ņ╣śļŻīņŚÉļÅä HS PDAĻ░Ć ņ¦ĆņåŹļÉśļŖö Ļ▓ĮņÜ░ ņłśņłĀņØä ĒĢśņśĆņ£╝ļ»ĆļĪ£, ņ¦ĆņŚ░ĒÅÉņćäĻĄ░ņŚÉ ņłśņłĀņØä ĒĢ£ ĒÖśņ×ÉĻ░Ć ļŹö ļ¦ÄņØ┤ ĒżĒĢ©ļÉśļŖö ņäĀĒāØĒÄĖĒ¢źņ£╝ļĪ£ ņØĖĒĢ┤ Ļ▓░Ļ│╝ņŚÉ ņśüĒ¢źņØä ņŻ╝ņŚłņØä ņłśļÅä ņ׳ļŗż.
Ļ▓░ļĪĀņĀüņ£╝ļĪ£, ļ»ĖņłÖņĢäņŚÉņä£ ļÅÖļ¦źĻ┤Ć ĒÅÉņćä ņŗ£ĻĖ░ļź╝ Ļ▓░ņĀĢĒĢ©ņŚÉ ņ׳ņ¢┤ņä£ ņŚ¼ļ¤¼ ņØĖņ×Éļź╝ Ļ│ĀļĀżĒĢ┤ņĢ╝ ĒĢśļ®░ ņŗ¼ĒĢ£ ņŗ¼ĒÅÉ ņ”ØņāüņØä ļÅÖļ░śĒĢ£ Ēü░ ļÅÖļ¦źĻ┤ĆņŚÉ ļīĆĒĢ£ ņ╣śļŻīļŖö ļČłĻ░ĆĒö╝ĒĢśĻ▓Āņ¦Ćļ¦ī ņĢĮļ¼╝ ņ╣śļŻīļéś ņłśņłĀņĀü ņ╣śļŻīņØś ĒÜ©Ļ│╝ņÖĆ ļČĆņ×æņÜ®ņØä Ļ│ĀļĀżĒ¢łņØä ļĢī ņāØĒøä ņ┤łĻĖ░ņŚÉ ņĀüĻĘ╣ņĀüņ£╝ļĪ£ ņĢĮļ¼╝ņØ┤ļéś ņłśņłĀļĪ£ ļÅÖļ¦źĻ┤ĆņØä ĒÅÉņćäĒĢśļŖö Ļ▓āņŚÉ ļīĆĒĢ┤ ļ│┤ļŗż ņŗĀņżæĒĢĀ ĒĢäņÜöĻ░Ć ņ׳ņ£╝ļ®░, ļ│┤ņĪ┤ņĀü ņ╣śļŻīļĪ£ ļÅÖļ¦źĻ┤ĆņØś Ēśłļźśļź╝ Ļ░Éņåīņŗ£ņ╝£ ļÅÖļ¦źĻ┤ĆĻ│╝ Ļ┤ĆļĀ©ļÉ£ ĒĢ®ļ│æņ”ØņØä ņżäņØ┤ļ®┤ņä£ ļ»ĖņłÖņĢäļź╝ ĒéżņÜ░ļŖö Ļ▓āļÅä ĒĢ®ļ”¼ņĀüņØĖ ļīĆņĢłņØ┤ ļÉĀ ņłś ņ׳ļŗżĻ│Ā ņāØĻ░üĒĢ£ļŗż.
ARTICLE INFORMATION
Ethical statement
This study was reviewed and approved by the Institutional Review Board of Inje University Busan Paik Hospital (identification code: 20-0046) in accordance with the Declaration of Helsinki. The Institutional Review Board waived the need for informed consent for this retrospective chart review.
Figure┬Ā1.
Patient flowchart. Abbreviations: GA, gestational age; PDA, Patent ductus arteriosus; HS, hemodynamically significant.
Table┬Ā1.
Demographic Factors
Table┬Ā2.
Outcomes
| Variable | Early closed group (n=40) | Delayed closed group (n=77) | P-value | P-value* |
|---|---|---|---|---|
| RDS | 40 (100.0) | 77 (100.0) | ┬Ł | ┬Ł |
| Surfactant re┬Łdosing | 4 (10.3) | 10 (13.3) | 0.635 | 0.842 |
| IVH (Ōēźgrade III) | 10 (25.0) | 10 (13.0) | 0.102 | 0.021 |
| Post┬Łclosure IVH | 7 (17.5) | 3 (3.9) | 0.013 | 0.011 |
| ROP (Ōēźstage II) | 11 (32.4) | 34 (44.7) | 0.222 | 0.453 |
| BPD (moderate to severe) | 5 (15.2) | 19 (26.8) | 0.191 | 0.384 |
| Mortality | 5 (12.5) | 7 (9.1) | 0.564 | 0.384 |
| NEC (Ōēźstage II) | 4 (10.0) | 7 (9.1) | 0.873 | 0.796 |
| Post┬Łclosure NEC | 3 (7.5) | 4 (5.2) | 0.618 | 0.677 |
| Total duration of mechanical ventilation (d) | 22.2┬▒19.7 | 37.1┬▒36.1 | 0.004 | 0.247 |
| Duration of invasive ventilation (d) | 17.3┬▒17.9 | 29.9┬▒29.1 | 0.004 | 0.218 |
| Hospital stay (d) | 75.7┬▒37.7 | 99.5┬▒39.9 | 0.002 | 0.056 |
Table┬Ā3.
Outcomes Stratified by Gestational Age
REFERENCES
1. Wyllie JP, Gupta S. Prophylactic and early targeted treatment of patent ductus arteriosus. Semin Fetal Neonatal Med 2018;23:250ŌĆō4.


2. Liu H, Manganiello V, Waleh N, Clyman RI. Expression, activity, and function of phosphodiesterases in the mature and immature ductus arteriosus. Pediatr Res 2008;64:477ŌĆō81.



3. Vettukattil JJ. Pathophysiology of patent ductus arteriosus in the preterm infant. Curr Pediatr Rev 2016;12:120ŌĆō2.


4. Clyman RI. Patent ductus arteriosus, its treatments, and the risks of pulmonary morbidity. Semin Perinatol 2018;42:235ŌĆō42.


5. Finlay ER, Subhedar NV. Pulmonary haemorrhage in preterm infants. Eur J Pediatr 2000;159:870ŌĆō1.



6. Havranek T, Rahimi M, Hall H, Armbrecht E. Feeding preterm neonates with patent ductus arteriosus (PDA): intestinal blood flow characteristics and clinical outcomes. J Matern Fetal Neonatal Med 2015;28:526ŌĆō30.


7. Mirza H, Laptook AR, Oh W, Vohr BR, Stoll BJ, Kandefer S, et al. Effects of indomethacin prophylaxis timing on intraventricular haemorrhage and patent ductus arteriosus in extremely low birth weight infants. Arch Dis Child Fetal Neonatal Ed 2016;101:F418ŌĆō22.



8. Noori S, McCoy M, Friedlich P, Bright B, Gottipati V, Seri I, et al. Failure of ductus arteriosus closure is associated with increased mortality in preterm infants. Pediatrics 2009;123:e138ŌĆō44.


9. Sinha R, Negi V, Dalal SS. An interesting observation of PDA closure with oral paracetamol in preterm neonates. J Clin Neonatol 2013;2:30ŌĆō2.



10. Foster M, Mallett LH, Govande V, Vora N, Castro A, Raju M, et al. Short-term complications associated with surgical ligation of patent ductus arteriosus in ELBW infants: a 25-year cohort study. Am J Perinatol 2019;Nov 4 [Epub]. https://doi.org/10.1055/s-0039-1698459.


11. Kaempf JW, Wu YX, Kaempf AJ, Kaempf AM, Wang L, Grunkemeier G. What happens when the patent ductus arteriosus is treated less aggressively in very low birth weight infants? J Perinatol 2012;32:344ŌĆō8.



12. Sung SI, Chang YS, Kim J, Choi JH, Ahn SY, Park WS. Natural evolution of ductus arteriosus with noninterventional conservative management in extremely preterm infants born at 23-28 weeks of gestation. PLoS One 2019;14:e0212256.



13. Sung SI, Choi SY, Park JH, Lee MS, Yoo HS, Ahn SY, et al. The timing of surgical ligation for patent ductus arteriosus is associated with neonatal morbidity in extremely preterm infants born at 23-25 weeks of gestation. J Korean Med Sci 2014;29:581ŌĆō6.



14. Jobe A. Respiratory distress syndrome: new therapeutic approaches to a complex pathophysiology. Adv Pediatr 1983;30:93ŌĆō130.


16. Papile LA, Burstein J, Burstein R, Koffler H. Incidence and evolution of subependymal and intraventricular hemorrhage: a study of infants with birth weights less than 1,500 gm. J Pediatr 1978;92:529ŌĆō34.


17. Walsh MC, Kliegman RM. Necrotizing enterocolitis: treatment based on staging criteria. Pediatr Clin North Am 1986;33:179ŌĆō201.



18. International Committee for the Classification of Retinopathy of Prematurity. The international classification of retinopathy of prematurity revisited. Arch Ophthalmol 2005;123:991ŌĆō9.


19. Ibrahim MH, Azab A, Kamal NM, Salama MA, Elshorbagy HH, Abdallah EA, et al. Outcomes of early ligation of patent ductus arteriosus in preterms, multicenter experience. Medicine (Baltimore) 2015;94:e915.



20. Liebowitz M, Koo J, Wickremasinghe A, Allen IE, Clyman RI. Effects of prophylactic indomethacin on vasopressor-dependent hypotension in extremely preterm infants. J Pediatr 2017;182:21ŌĆō7.


21. Liebowitz M, Clyman RI. Prophylactic indomethacin compared with delayed conservative management of the patent ductus arteriosus in extremely preterm infants: effects on neonatal outcomes. J Pediatr 2017;187:119ŌĆō26.



22. Schena F, Francescato G, Cappelleri A, Picciolli I, Mayer A, Mosca F, et al. Association between hemodynamically significant patent ductus arteriosus and bronchopulmonary dysplasia. J Pediatr 2015;166:1488ŌĆō92.


23. Sellmer A, Bjerre JV, Schmidt MR, McNamara PJ, Hjortdal VE, Host B, et al. Morbidity and mortality in preterm neonates with patent ductus arteriosus on day 3. Arch Dis Child Fetal Neonatal Ed 2013;98:F505ŌĆō10.


24. Fonseca E, Georgiev SG, Gorenflo M, Loukanov TS. Patent ductus arteriosus in preterm infants: benefits of early surgical closure. Asian Cardiovasc Thorac Ann 2014;22:391ŌĆō6.


25. Bourgoin L, Cipierre C, Hauet Q, Basset H, Gournay V, Roze JC, et al. Neurodevelopmental outcome at 2 years of age according to patent ductus arteriosus management in very preterm infants. Neonatology 2016;109:139ŌĆō46.


26. Benitz WE, Committee on Fetus and Newborn, American Academy of Pediatrics. Patent ductus arteriosus in preterm infants. Pediatrics 2016;137:e20153730.

27. Slaughter JL, Reagan PB, Newman TB, Klebanoff MA. Comparative effectiveness of nonsteroidal anti-inflammatory drug treatment vs no treatment for patent ductus arteriosus in preterm infants. JAMA Pediatr 2017;171:e164354.



28. Weisz DE, Mirea L, Resende MHF, Ly L, Church PT, Kelly E, et al. Outcomes of surgical ligation after unsuccessful pharmacotherapy for patent ductus arteriosus in neonates born extremely preterm. J Pediatr 2018;195:292ŌĆō6.


-
METRICS

-
- 1 Crossref
- 6,675 View
- 118 Download
- Related articles in NM
-
Risk Factors of Paternt Ductus Arteriosus in Very Low Birth Weight infants.1997 November;4(2)






